Dosage de l'ammoniac dans la fumée principale de tabac
Santé Canada
T-101 31 décembre 1999
Table des matières
- Portée
- Normes applicables
- Définitions
- Résumé de la méthode
- Appareillage et équipement
- Réactifs et matériel
- Préparation de la verrerie
- Préparation des solutions
- Préparation des étalons
- Échantillonnage
- Préparation des produits du tabac
- Préparation de la machine à fumer
- Production des échantillons
- Analyse des échantillons
- Contrôle de la qualité
- Modifications pour le fumage dans des conditions intenses
- Références
- Annexe
1 Portée
- La présente méthode s'applique à la séparation et au dosage par chromatographie d'échange d'ions de l'ammoniac présent dans la fumée principale de tabac.
2 Normes applicables
- American Society for Testing and Materials (ASTM) : Méthode D 1193-77 - Standard Specifications for Reagent Water, Version 1977.
- Méthode d'essai T-115 de Santé Canada - Dosage du goudron, de l'eau, de la nicotine et du monoxyde de carbone dans la fumée principale de tabac, 1999-12-31.
3 Définitions
- Pour une définition des termes utilisés dans le présent document, se reporter à la méthode T-115.
4 Résumé de la méthode
- 10 cigarettes* sont fumées sur une machine à fumer rotative et la fumée est acheminée dans un disque filtrant (tampon) en fibre de verre, de 92 mm, puis dans deux flacons laveurs contenant 15 mL de H2SO4 0,1 N et disposés en série entre le tampon et la seringue d'aspiration. Le tampon est placé dans un erlenmeyer de 125 mL (après pesée en vue de déterminer la quantité de MPT), dans lequel on ajoute également le contenu des deux flacons laveurs.
- Le fumage mécanique peut aussi être réalisé au moyen d'une machine à fumer de type linéaire. Dans ce cas, 10 cigarettes* sont fumées et la fumée est acheminée dans un disque filtrant en fibre de verre, de 44 mm, et un seul flacon laveur contenant
30 mL de H2SO4 0,1 N et disposé entre le tampon et la seringue d'aspiration. Dans ce cas, le tampon doit être remplacé après cinq cigarettes afin d'éviter qu'il ne laisse passer des substances qu'il devrait normalement
piéger (des taches brunes apparaissant au dos du tampon indiquent qu'il est saturé).
*Pour les autres produits du tabac, retenir un nombre tel que le tampon ne soit pas saturé.
Nota : Il faut d'abord évaluer la capacité des flacons laveurs requis en montant un circuit comportant trois flacons laveurs disposés en série. Il faut analyser séparément le contenu de tous les éléments du circuit afin de déterminer leur efficacité de piégeage. Si la quantité de produit se retrouvant dans le deuxième et le troisième flacons laveurs est supérieure à 3 % de la quantité dans le premier, il faut inclure ces flacons laveurs dans le circuit. L'efficacité de piégeage peut différer légèrement selon la conception du flacon laveur. - Le tampon (ou les tampons) est extrait pendant 30 minutes avec la solution diluée placée dans le flacon laveur monté sur un agitateur oscillant. Ce mélange est ensuite filtré sur une seringue-filtre de 0,45 μm, dans un flacon à scintillation. L'échantillon peut être conservé dans ce flacon à 4 °C pendant une période pouvant atteindre 48 heures.
- On transfère ensuite une portion de l'échantillon filtré dans un flacon pour échantillonneur automatique; cette portion peut être analysée directement par chromatographie d'échange de cations.
- On injecte 35 μL de l'échantillon sur une colonne d'analyse par échange de cations. Cette colonne permet de séparer les ions ammonium et les cations monovalents grâce à des groupements d'acide carboxylique/acide phosphonique. Afin de séparer convenablement le sodium de l'ammonium, qui sera dosé, on utilise comme phase mobile une solution 0,003 N (normal) d'acide méthanesulfonique. Après élution de l'ion ammonium, on ajoute du H2SO4 à un gradient de concentrations allant de 0,2 N à 0,05 N, pour éliminer tout cation divalent et toute amine quaternaire susceptibles d'être présents dans l'échantillon.
- Les cations sont détectés à l'aide d'un détecteur de conductivité compensée, fonctionnant en mode eau externe. Cette méthode de détection permet de réduire la conductivité de fond attribuable à la phase mobile, et ainsi d'accroître la sensibilité du détecteur à l'analyte.
- On détermine la quantité d'ammoniac à partir d'une courbe d'étalonnage établie à l'aide de cinq étalons externes, en utilisant comme réponse la hauteur du pic correspondant au sulfate d'ammonium. On détermine la quantité d'ammoniac par cigarette
en calculant la quantité d'ammoniac présente dans la solution analysée, puis en multipliant celle-ci par le facteur approprié (volume de solution dans le flacon laveur × dilutions) et en la divisant par le nombre de cigarettes fumées.
Nota : L'analyse et l'évaluation de certains produits à l'aide de cette méthode d'essai peuvent nécessiter l'utilisation de substances ou d'équipement potentiellement dangereux. Le présent document n'entend pas répondre à tous les aspects concernant la sécurité de son utilisation. Avant d'utiliser cette méthode d'essai, toute personne a la responsabilité de consulter les autorités compétentes et de prendre des mesures de protection de la santé et des mesures de sécurité qui tiennent compte des règlements en vigueur.
5 Appareillage et équipement
- Équipement nécessaire au conditionnement, tel que défini dans la méthode T-115.
- Équipement nécessaire au marquage de la longueur des mégots, tel que défini dans la méthode T-115.
- Équipement nécessaire au fumage mécanique des produits du tabac, tel que défini dans la méthode T-115.
- Balance analytique, précise à au moins quatre places décimales.
- Brucelles et gants propres pour le transfert des tampons.
- Erlenmeyers de 125 mL en polyméthylpentène (PMP), munis d'un bouchon à vis.
- Agitateur oscillant à vitesse constante.
- Seringue-filtre avec filtre en fibre de verre (25 mm × 0,45 µm).
- Flacons laveurs de 70 mL, sans fritté.
- Fioles jaugées de 100 mL.
- Seringue jetable de 5 cm3.
- Flacons à vis de 7 mL, avec bouchons à vis recouverts d'aluminium.
- Flacons pour échantillonneur automatique, avec bouchons et septums recouverts de téflon.
- Appareil pour chromatographie liquide haute performance (CLHP) muni de :
- Échantillonneur automatique réfrigéré avec boucle d'injection de 100 μL à remplissage partiel.
- Système pour gradient ternaire.
- Chauffage de la colonne.
- Détecteur de conductivité Dionex ED-40 ou l'équivalent.
- Piège à cations Dionex CTC-1 ou l'équivalent.
- Compensateur de conductivité Dionex CSRS-II en mode eau externe ou l'équivalent.
- Système de collecte des données.
- Colonne d'analyses échangeuse de cations Dionex IonPac CS12A (250 mm × 4 mm) ou l'équivalent.
- Colonne de garde échangeuse de cations Dionex IonPac CG12A (50 mm × 4 mm) ou l'équivalent.
6 Réactifs et matériel
Nota : Tous les réactifs doivent être, au minimum, des réactifs de qualité analytique.
- Sulfate d'ammonium (> 99 %).
- Acide sulfurique (96 %).
- Acide méthanesulfonique (MSA) (100 %).
- Eau de type I (satisfaisant à la norme D 1193 de l'ASTM) .
7 Préparation de la verrerie
- Le lavage et la séchage de la verrerie doivent être effectués de manière à ce que celle-ci ne cause pas de contamination.
- Tout juste avant de s'en servir, tous les flacons laveurs doivent être rincés deux fois avec du H2SO4 0,1 N, puis trois fois avec de l'eau de type I.
8 Préparation des solutions
- Solution d'acide sulfurique 0,10 N - Solution pour flacons laveurs
- Ajouter avec soin 5,108 g de H2SO4 Suprapur (96 % pds/pds) dans 900 mL d'eau de type I.
- Mélanger et diluer jusqu'à 1 L avec de l'eau de type I.
- Solution d'acide sulfurique 0,20 N - Solution C (chromatographie d'échange d'ions)
- Ajouter avec soin 10,216 g de H2SO4 Suprapur (96 % pds/pds) dans 900 mL d'eau de type I.
- Mélanger et diluer jusqu'à 1 L avec de l'eau de type I
- Solution de MSA 0,003 N - Solution A (chromatographie d'échange d'ions)
- Ajouter avec soin 0,2883 g d'acide méthanesulfonique (MSA) dans 900 mL d'eau de type I.
- Mélanger et diluer jusqu'à 1 L avec de l'eau de type I.
9 Préparation des étalons
- 9.1 Solution mère primaire d'ammonium :
- Peser avec précision 0,20 g de sulfate d'ammonium dans une fiole jaugée de 50 mL.
- Dissoudre dans du H2SO4 0,10 N.
- Mélanger et diluer à 50 mL avec de l'eau de type I.
- Préparer une nouvelle solution tous les dix jours.
Nota : Cette solution mère contient 1,0898 mg/mL de NH4+ .
- Étalons de travail
Le tableau suivant présente l’ensemble des concentrations des étalons 0 à 6 en µg/mL; le volume correspondant de la solution mère primaire; et le volume final et la concentration des solutions nécessaires pour produire chaque étalon.
9.2 Étalons de travail Étalon No Volume de solution mère primaire (μL) Volume final Concentration [µg/mL] 0 0 25 0,000 1 250 25 10,898 2 175 25 7,6283 3 75 25 3,2693 4 75 50 1,6346 5 50 100 0,5449 6 20 100 0,2180
Nota : Tous ces étalons de travail sont dilués de manière à obtenir une concentration de 50 mN de H2SO4. Préparer de nouveaux étalons de travail tous les cinq jours.
10 Échantillonnage
- L'échantillonnage des produits du tabac à analyser doit être effectué conformément à la méthode T-115.
11 Préparation des produits du tabac
- Le conditionnement du produit doit être effectué conformément à la méthode T-115.
- La longueur de mégot des cigarettes, des équivalents-cigarettes, des bidis, des kreteks et des cigares doit être indiquée conformément à la méthode T-115.
- La préparation des cigarettes à être fumées dans des conditions intenses doit être effectuée conformément à la méthode T-115.
12 Préparation de la machine à fumer
-
Conditions ambiantes
- Les conditions ambiantes de fumage doivent être conformes à celles de la méthode T-115.
-
Conditions relatives à la machine à fumer
- Les conditions relatives à la machine à fumer doivent être conformes à celles de la méthode T-115, sauf pour les modifications détaillées ciaprès :
- Conditions spécifiques au fumage sur une machine rotative
- À l'aide d'un tube en tygon, brancher deux flacons laveurs de 70 mL contenant chacun 15 mL de H2SO4 0,1 N, entre le filtre de 92 mm et le porte-filtre (filtre en fibre de verre) de garde sur le tableau pneumatique.
- Régler le tableau pneumatique de la machine à fumer de manière à obtenir un volume de bouffée de 35 mL (± 0,2 mL) (avec le filtre et les flacons laveurs en place) et un temps de balayage de 1,85 secondes, en utilisant le chronomètre fourni à cet effet pour mesurer le temps de balayage réglé.
-
Conditions spécifiques au fumage sur une machine linéaire
- Brancher un flacon laveur de 70 mL, contenant 30 mL de H2SO4 0,1 N, entre le porte-filtre de 44 mm et le solénoïde de la machine à fumer.
- Régler la machine à fumer de manière à obtenir un volume de bouffée de 35 mL (± 0,2 mL) (avec le filtre et le flacon laveur en place).
13 Production des échantillons
- Les conditions de fumage et de piégeage sont celle définies dans la méthode T-115.
- Une fois le fumage terminé, le porte-filtre de 92 mm est pesée et son poids est consigné. Le taux de MPT par cigarette est calculé à l'aide de la formule donnée dans la section « Calculs ».
Nota : Le fumage sur une machine linéaire requiert les modifications appropriées mentionnées à la section 12.2.3. En plus de ces modifications, le filtre en fibre de verre doit être remplacé après cinq cigarettes afin d'éviter qu'il y ait non-piégeage pour des raisons de saturation. Une seule bouffée est aspirée à vide à la fin du fumage de chaque cigarette et deux bouffées supplémentaires sont aspirées avant de retirer le porte-filtre (à la fin de la cinquième et de la 10e cigarettes).
- Une fois le fumage terminé, le porte-filtre de 92 mm est pesée et son poids est consigné. Le taux de MPT par cigarette est calculé à l'aide de la formule donnée dans la section « Calculs ».
14 Analyse des échantillons
- Extraction des filtres
- Une fois le fumage terminé, retirer le filtre de 92 mm (ou de 44 mm, dans le cas des machines linéaires) et le plier en quatre.
- Placer le tampon (ou les tampons, dans le cas des machines linéaires) dans un erlenmeyer de 125 mL.
- Ajouter la solution contenue dans le ou les flacons laveurs.
- Rincer les flacons laveurs avec un volume égal d'eau (p. ex., pour un volume de 30 mL dans le flacon laveur, utiliser 30 mL d'eau de type l'ajouter dans l'erlenmeyer.
- Boucher l'erlenmeyer et l'agiter pendant 30 minutes sur un agitateur oscillant.
- Purification des échantillons
- Filtrer la solution avec une seringue-filtre et récupérer le filtrat dans un flacon. Rincer d'abord le flacon avec environ 1 mL d'échantillon.
- Transférer l'extrait filtré dans un flacon pour échantillonneur automatique (H2SO4 50 mN).
- Les échantillons peuvent être conservés à 4 °C jusqu'à 48 heures avant l'analyse.
- Analyse - Analyse par CLHP
- Paramètres pour le Dionex ED-40
Compensateur de conductivité (SRS) : 100 mA.
Échelle : 20 µS.
Signal : déport.
Mise à zéro : 1 % de la pleine échelle. -
Échantillonneur automatique : volume injecté
- Faire les analyses en utilisant une boucle d'échantillonnage de 100 μL et un volume d'injection réglé à 35 μL, avec un volume de lavage de 60 μL.
- Température de la colonne : 30 °C.
- Phase mobile et gradient (système ternaire à gradient)
Solvant A : MSA 0,003 N.
Solvant B : Eau de type I.
Solvant C : H2SO4 0,2 N.
Débit : 1,5 mL/minute.
Gradient : Des ajustements mineurs peuvent être nécessaires selon la condition de la colonne et la résolution des analytes.
Le tableau suivant présente des renseignements sur les phases mobiles et le gradient utilisés pour l’analyse par CLHP. Trois phases mobiles ont été utilisées : le solvant A (MSA 0,003 N), le solvant B (eau de type I) et le solvant C (H2SO4 0,2 N). Les analytes ont été séparés en 25 minutes par plusieurs gradients pendant la période d’équilibrage de 8 minutes.
Temps (minutes) Composition % A % B % C 0.00 100 0 0 13.00 100 0 0 13.01 0 80 20 14.00 0 80 20 14.01 0 90 10 19.00 0 90 10 19.01 0 99 1 20.00 0 99 1 25.00 99 1 0 25.00 Fin de l'analyse : Équilibrer
Temps d’équilibrage : 9,00 minutes
- Paramètres pour le Dionex ED-40
- Calculs
-
Détermination du facteur de réponse (FR)
- Procéder à un premier étalonnage en analysant les étalons préparés; commencer par les concentrations élevées et progresser vers les concentrations faibles (injecter le tout premier étalon au moins deux fois jusqu'à l'obtention d'une réponse et d'un temps de rétention constants).
- Préparer une courbe d'étalonnage en traçant la concentration des ions NH4+ dans l'étalon en fonction de la hauteur du pic fourni par le détecteur de conductivité.
- Le facteur de réponse est égal à la pente de la droite calculée par régression linéaire (hauteur / concentration).
- Calcul de la teneur en ion ammonium
NH4+ [μg/cigarette] = [hauteur de pic × volume de solvant d'extraction (mL) × volume final (mL)] / [FR × nbre de cigarettes fumées × volume de la portion analysée (mL)]
dans laquelle le volume de la portion analysée (mL) est le volume transféré quantitativement dans le flacon de l'échantillonneur automatique (si nécessaire). - Calcul de la teneur en ammoniac
NH3 [μg/cigarette] = NH4+ [μg/cigarette] × (17/18)
dans laquelle le rapport 17/18 permet de corriger pour tenir compte du poids moléculaire. - Calcul de la quantité de matière particulaire totale (MPT)
MPT [mg/cigarette] = ([filtre + porte-filtreaprès fumage (g) − (filtre + porte-filtreavant fumage)(g)]) × 1000 mg/g.
-
Détermination du facteur de réponse (FR)
15 Contrôle de la qualité
- Chromatogramme typique
- Voir l'annexe 1.
- Paramètres de contrôle typiques
- Blanc de réactifs : Avant de traiter un échantillon, l'analyste doit établir, par analyse d'un blanc de réactifs, que le système d'analyse, la verrerie et les réactifs ne constituent pas une source de perturbation.
- Pour chaque série d'analyses, il faut analyser un blanc de réactifs (BR) et un blanc fortifié (BF). Le blanc et l'échantillon dopé doivent être soumis à toutes les étapes de la préparation et du dosage des échantillons.
- Matrice fortifiée (MF) : Analyser une matrice fortifiée pour identifier les interférences de matrice. Fortifier un échantillon de concentration connue et déterminer le % de récupération.
- Taux de récupération et niveaux de contamination
- Les taux de récupération typiques des blancs fortifiés (BF) et des matrices fortifiées (MF) se situent dans la gamme de 85 - 110 %, lorsqu'une solution dopée (ou un échantillon) est soumise au processus complet d'extraction.
- Les résultats obtenus avec des blancs de réactifs (BR) typiques varient de 0 μg/cigarette. Normalement, une contamination de ce type est associée à une contamination du tampon-filtre au cours du conditionnement ou à un nettoyage inadéquat de la verrerie.
- Limites de détection de la méthode (LDM) / limite de dosage (LDD)
- Déterminer la limite de détection de la méthode (LDM) en analysant l'étalon le moins concentré, comme s'il s'agissait d'un échantillon inconnu, au moins 10 fois sur une période de plusieurs jours. La LDM est égale à trois fois l'écart-type de ces résultats.
- On peut modifier la LDM (en ng/cigarette) en changeant le nombre de cigarettes fumées et les volumes utilisés pour l'extraction et la purification.
- Déterminer la limite de dosage (LDD) pratique en analysant l'étalon le moins concentré, comme s'il s'agissait d'un échantillon inconnu, au moins 10 fois sur une période de plusieurs jours. La LDD est égale à 10 fois l'écart-type de ces résultats.
- Dans le cas d'échantillons véritables, la LDM et la LDD dépendent de la résolution chromatographique et de la quantité d'ions sodium dans l'échantillon, car la trainée derrière un énorme pic correspondant au sodium peut masquer les ions ammonium présents.
- Stabilité des réactifs et des échantillons
- À tous les 10 jours, préparer de nouveaux étalons primaires et les conservert à 4 °C.
- À chaque semaine, préparer de nouveaux étalons de travail à partir de la solution mère et les conserver à 4 °C.
- Les échantillons dilués doivent être analysés dans les 48 heures suivant leur préparation.
16 Modifications pour le fumage dans des conditions intenses
- Dans des conditions de fumage intense, fumer cinq cigarettes au lieu de 20.
17 Références
- Risner, C.H. et J.M. Conner. Collection of Ammonia in Indoor Air by Means of a Weak Cation Exchange Cartridge, Environmental Toxicology and Chemistry, vol. 10, 1991, p. 1417-1423.
- Nanni, E.J., Lovette, M.E., Hicks, R.D., Fowler, K.W. et M.F. Borgerding. Separation and Quantitation of Monovalent and Cationic Species in mainstream Cigarette Smoke Aerosols by High-Performance Ion Chromatography, Journal of Chromatographic Science, vol. 28, août 1990.
- IonPac CS12A Analytical Column, Installation Instructions and Troubleshooting Guide, Document No. 031132, Revision 01, Dionex Corporation, 1995.
Annexe
Annexe 1 : Chromatogramme typique
Cette figure est une superposition des chromatogrammes d’un étalon et d’une cigarette témoin. Elle fait ressortir un décalage de 5 % des pics de la cigarette témoin.
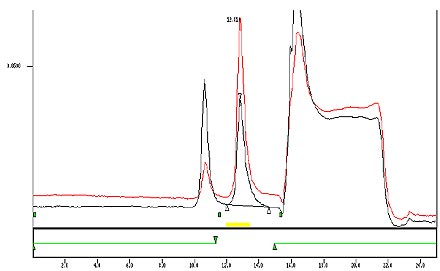
Superposition des chromatogrammes obtenus avec un étalon et avec une cigarette témoin, avec un décalage de 5 %.