Dosage de l'acide sorbique dans le tabac entier
Santé Canada
T-313 31 décembre 1999
Table des matières
- Portée des applications
- Méthodes applicables
- Résumé de la méthode
- Appareillage et équipement
- Réactifs et matériel
- Préparation de la verrerie
- Préparation des solutions
- Préparation des étalons
- Préparation des produits du tabac
- Préparation de la machine à fumer
- Préparation des échantillons
- Analyse des échantillons
- Contrôle de la qualité
- Références
- Annexe
1 Portée des applications
- La présente méthode permet de doser l'acide sorbique ajouté au tabac entier comme agent antimicrobien, à l'aide d'un chromatographe liquide à haute performance (CLHP) en phase inversée muni d'un détecteur à ultraviolet (détecteur UV). Elle est destinée à être utilisée pour l'analyse de routine sans exiger la formation d'un dérivé. Cette méthode s'applique au tabac traité pour cigarette, au tabac coupe fine, au tabac à priser, aux échantillons de cigare et au tabac pour pipe.
- Cette méthode ne permet pas de distinguer l'acide sorbique ajouté de l'acide sorbique présente naturellement (le cas échéant) dans le tabac entier.
2 Méthodes applicables
- American Society for Testing and Materials (ASTM) : Méthode D 1193-77 Standard Specification for Reagent Water, Version 1977.
- Méthode d'analyse T-115 de Santé Canada : Dosage du goudron, de l'eau, de la nicotine et du monoxyde de carbone dans la fumée principale du courant, 1999-12-31.
3 Résumé de la méthode
- Le tabac entier est extrait avec 50 mL d'eau chaude dans un agitateur à ultrasons.
- La suspension obtenue est centrifugée, puis décantée dans une fiole jaugée.
- Le surnageant est refroidi, complété au trait de jauge, filtré avec une seringuefiltre, puis le filtrat est récupéré dans un flacon de 1,5 mL pour échantillonneur automatique et analysé par CLHP en phase inversée.
- La phase mobile est contrôlée par un détecteur UV et l'acide sorbique est dosé par comparaison avec des étalons externes.
Nota : L'analyse et l'évaluation de certains produits à l'aide de cette méthode peuvent nécessiter l'utilisation de substances ou d'équipement potentiellement dangereux. Le présent document n'entend pas répondre à tous les aspects concernant la sécurité de son utilisation. Avant d'utiliser cette méthode normalisée, toute personne a la responsabilité de consulter les autorités compétentes et de prendre des mesures de protection de la santé et des mesures de sécurité qui tiennent compte des règlements en vigueur.
4 Appareillage et équipement
- Fiole jaugée de 2000 mL.
- Fioles jaugées ambres de 100 mL.
- Fioles jaugées ambres de 10 mL.
- Éprouvette graduée de 50 mL, en verre.
- Tubes à culture de 200 × 25 mm, avec bouchons à vis.
- Bouchons en polypropylène, blancs, sans garnitures.
- Micropipettes, pour la préparation des étalons d'analyse.
- Distributrice genre Dispensette, 10 - 50 mL.
- Micropipettes de 200 µL et de 25 µL.
- Filtre-seringue.
- Seringues jetables.
- Flacons pour échantillonneur automatique .
- Bouchons à vis.
- Septa, 8 mm, à revêtement en téflon, 60 mil.
- Lunettes de protection.
- Poires en caoutchouc.
- Parafilm.
- Centrifugeur .
- Broyeur fonctionnant en discontinu (Robot Coupe RS1-2V ou l'équivalent).
- Mélangeur Vortex.
- Balance analytique précise à quatre places décimales.
- pH-mètre.
- Mélangeur à ultrasons.
- Système de chromatographie liquide à haute performance, piloté par ordinateur, comprenant :
- Système d'alimentation en solvant - pompe à gradient ternaire.
- Échantillonneur automatique avec boucle d'échantillonnage de 20 µL.
- Détecteur UV Varian ou l'équivalent.
- Poste de travail.
- Colonne RP 18e.
- Colonne de garde jetable.
5 Réactifs et matériel
- Sorbate de potassium, pureté d'au moins 99 %.
- Orthophosphate monopotassique, pureté d'au moins 99 %.
- Acide phosphorique, pureté de 85 %.
- Eau de type I conforme à la norme D1193 de l'ASTM.
- Méthanol, distillé en verre.
- Pipettes Pasteur, en verre, jetables.
- Gants jetables.
6 Préparation de la verrerie
- Le lavage et le séchage doivent être effectués de manière à ce que la verrerie ne constitue pas une source de contamination.
7 Préparation des solutions
- Cette étape ne s'applique pas à la présente méthode.
8 Préparation des étalons
- Étalons primaires (1o) de sorbate
- Peser 100 mg de sorbate de potassium dans une fiole jaugée de 100 mL.
- Diluer avec de l'eau de type I.
- Étalons de travail
- Prélever des volumes appropriés (de 0,05 à 1,0 mL) de solution étalon primaire de sorbate et diluer jusqu'à 10 mL avec de l'eau de type 1, pour obtenir des étalons de travail dont la concentration approximative de sorbate se situe dans la plage de 5 - 100 ppm.
Le tableau suivant présente les détails de la préparation des étalons des étalons d’acide sorbique, y compris le blanc 0 et les étalons 1 à 5. Il indique le volume initial de la solution mère d’acide sorbique, le volume final de l’échantillon et la concentration finale de sorbate.
Étalons de travail d'acide sorbique Étalon Vol. (mL) 1°
d'acide
sorbiqueVolume Finale
mLSorbate
[mg/mL] (ppm)Blanc 0 0 10 0,0 Étalon 1 0,050 10 5,0 Étalon 2 0,100 10 10,0 Étalon 3 0,250 10 25,0 Étalon 4 0,5 10 50,0 Étalon 5 1,0 10 100,0
Nota 1 : La concentration de sorbate varie selon la concentration exacte de la solution étalon primaire préparée. - Transvider dans des flacons ambres de 1,5 mL pour échantillonneur automatique. Rincer d'abord les flacons, puis les remplir de manière à réduire le plus possible l'espace libre.
- Placer les flacons dans un support pour flacons et conserver à 4 °C, à l'obscurité, jusqu'au moment de l'analyse.
- Préparer de nouvelles solutions étalons de travail de sorbate à tous les cinq jours ouvrables.
- Prélever des volumes appropriés (de 0,05 à 1,0 mL) de solution étalon primaire de sorbate et diluer jusqu'à 10 mL avec de l'eau de type 1, pour obtenir des étalons de travail dont la concentration approximative de sorbate se situe dans la plage de 5 - 100 ppm.
9 Préparation des produits du tabac
- Préparation des échantillons
- Conditionner les produits du tabac conformément à la méthode T-115.
- Retirer le tabac entier nécessaire à l'analyse de son emballage d'origine et l'examiner pour voir s'il renferme des matières étrangères.
10 Préparation de la machine à fumer
- Cette étape ne s'applique pas à la présente méthode.
11 Préparation des échantillons
- À l'aide d'un broyeur fonctionnant en discontinu, broyer finement (jusqu'à une granulométrie de 20 mailles) plusieurs grammes de tabac.
- Peser avec précision 1 g de tabac finement broyé dans un tube à culture en verre, de 200 × 25 mm, muni d'un bouchon à vis.
- Ajouter 30 mL d'eau de type I chaude (50 °C) et traiter dans un mélangeur à ultrasons pendant 30 minutes à 50 °C.
- Centrifuger à environ 1200 tr/minute pendant 10 minutes, puis décanter l'eau dans une fiole jaugée de 100 mL.
- Répéter les étapes 11.3 à 11.5 avec une autre portion de 1 g de tabac, puis décanter dans la même fiole jaugée, en réunissant ainsi l'extrait de 2 g de tabac.
- Laisser l'échantillon refroidir, puis compléter avec de l'eau de type I.
- Bien mélanger, puis à l'aide d'un filtre-seringue jetable fixé à une seringue jetable, filtrer une portion dans un flacon ambre pour échantillonneur automatique. Boucher et conserver à 4 °C.
12 Analyse des échantillons
- Analyse par CLHP en phase inversée
- Conditions chromatographiques (analyse en phase inversée)
- Température de la colonne : 30 °C.
- Phase mobile : Réactifs.
Solvant A : Méthanol, filtrer et dégazer (par barbotage d'hélium UHP).
Solvant B : Préparer 2 L d'une solution d'isopropanol à 1 %, régler le pH à 2,3 avec de l'acide phosphorique, filtrer et dégazer (par barbotage d'hélium UHP). - Lavage de l'échantillon : Solvant A.
- Phase mobile : Gradient - isocratique.
Débit 1,0 mL/minute
Temps (minutes) Composition % A % B % C 0,0 35 65 0 20,0 35 65 0 Fin de la méthode 35 65 0 (Temps d'équilibrage : cinq minutes).
- Charger les flacons d'échantillons dans l'échantillonneur automatique en insérant une solution étalon à tous les 10 échantillons; de plus, les quantités doivent être telles que les échantillons chargés ne restent pas à la température ambiante plus de 24 heures au total (parties 10 - 11).
- Procéder à l'analyse en injectant 20 µL de chaque échantillon sur la colonne du CLHP. Le profil d'élution devrait être semblable à celui illustré à la figure 1.
- Conditions chromatographiques (analyse en phase inversée)
- Calculs
- Courbe d'étalonnage
- Injecter 20 µL de chaque solution étalon de travail dans le CLHP. Analyser chaque étalon en double. Le profil d'élution devrait être semblable à celui illustré à la figure 2.
- Préparer une courbe d'étalonnage en traçant la concentration des étalons en fonction de l'aire sous les pics correspondants.
- Déterminer le facteur de réponse à partir de la courbe d'étalonnage.
- Dosage des échantillons
- Déterminer la quantité d'acide sorbique dans les échantillons par la méthode des étalons externes.
- Identifier les pics par comparaison des temps de rétention avec ceux des étalons, et par dopage des échantillons.
- Détermination de la teneur en sorbitol, en µg/cigarette
Sorbitol [µg/g] = [surface sous le pic / facteur de réponse] × [mL de solution / poids de tabac]
- En entrant le multiplicateur approprié (volume total de dilution de l'échantillon original, en mL) et le diviseur approprié (poids de l'échantillon original, en g), on obtient automatiquement la teneur en sorbitol, en µg/g.
- Pour convertir cette teneur en pourcentage (%), il faut diviser le résultat en µg/g par 10 000.
- Tous les résultats sont exprimés pour le tabac conditionné. On peut les exprimer en matière sèche en utilisant la valeur appropriée pour la teneur en humidité.
- Courbe d'étalonnage
13 Contrôle de la qualité
- Chromatogramme typique
- Voir la figure 1.
- Taux de récupération et niveaux de contamination
- Chaque série d'analyses du tabac entier doit comprendre :
- Un blanc de réactif (BR) pour évaluer l'importance des perturbations dues à la verrerie et aux effets de l'analyseur.
- Un blanc fortifié (BF) pour évaluer l'importance de la perte possible d'analyte.
- Une matrice fortifiée (MF) pour évaluer les effets perturbants de la matrice. Pour ce faire, doper un échantillon véritable avec une quantité connue et déterminer le taux de récupération (en %).
- Chaque série d'analyses du tabac entier doit comprendre :
- Limite de détection de la méthode (LDM) et limite de dosage (LDD)
- Limite de détection de la méthode (LDM)
Déterminer la limite de détection de la méthode en analysant l'étalon le moins concentré, comme s'il s'agissait d'un échantillon, au moins 10 fois sur une période de plusieurs jours. La LDM est égale à trois fois l'écarttype de ces résultats. - Limite de dosage (LDD)
Déterminer la limite de dosage en analysant l'étalon le moins concentré, comme s'il s'agissait d'un échantillon, au moins 10 fois sur une période de plusieurs jours. La LDD est égale à 10 fois l'écart-type de ces résultats.
- Limite de détection de la méthode (LDM)
- Stabilité des réactifs et des solutions
- Préparer de nouvelles solutions étalons primaires de sorbitol à chaque semaine.
- Préparer de nouveaux étalons de travail et de nouvelles solutions d'extraction à chaque semaine.
- Analyser tous les échantillons dans les 24 heures.
14 Références
- AOAC Official Method 974.10, « Fatty Acids (Volatile) in Eggs, Gas Chromatographic Method », AOAC Official Methods of Analysis, 1995, ch. 34, p. 10-12.
- Rosa, Nestor et C.W. H. Caughill. « Effect of Aqueous Ethanol, Sample Particle Size, and Temperature on Extractability of Soluble Acids from Tobacco ». Tobacco Science, janvier 1984.
15 Annexe
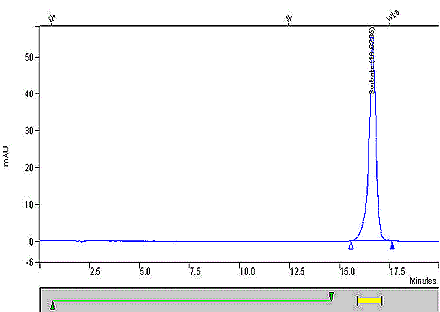
Figure 1 : Chromatogramme CLHP typique obtenu lors du dosage du sorbate dans un échantillon de tabac
La figure suivante est un chromatogramme typique d’un échantillon de tabac analysé par chromatographie liquide haute performance de dosage du sorbate. L’intensité de l’absorbance en milli-unités d’absorbance est présentée en fonction de temps écoulé (en minutes).
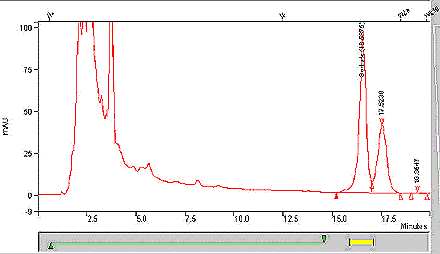
Figure 2 : Chromatogramme CLHP typique obtenu lors de l'analyse d'un étalon de sorbate
La figure suivante est un chromatogramme typique d’un étalon de sorbate analysé par chromatographie liquide haute performance. L’intensité de l’absorbance en milli-unités d’absorbance est présentée en fonction de temps écoulé (en minutes).