Dosage de l'ammoniac dans le tabac entier
Santé Canada
T-302 31 décembre 1999
Table des matières
- Portée des applications
- Méthodes applicables
- Résumé de la méthode
- Appareillage et équipement
- Réactifs et matériel
- Préparation de la verrerie
- Préparation des solutions
- Préparation des étalons
- Échantillonnage
- Analyse des échantillons
- Contrôle de la qualité
- Références
- Annexe
1 Portée des applications
- Cette méthode s'applique à la séparation et au dosage de l'ammoniac dans le tabac entier par chromatographie liquide à haute pression (CLHP).
2 Méthodes applicables
- American Society for Testing and Materials (ASTM) : Méthode D 1193-77 - Standard Specification for Reagent Water, Version 1977.
- Méthode d'essai de Santé Canada T-115 - Dosage du goudron, de la nicotine et du monoxyde de carbone dans la fumée principale de tabac, 1999-12-31.
3 Résumé de la méthode
- Environ 3 g de tabac entier sont placés dans un flacon à scintillation taré, puis lyophilisés pendant 48 heures. Après le calcul de son degré d'humidité, l'échantillon est broyé avec un broyeur de laboratoire muni d'un tamis no 40 (40 mailles au pouce carré).
- On pèse exactement 100 mg de tabac lyophilisé dans un erlenmeyer de 16 mL. L'échantillon est extrait avec 10 mL de H2SO4 0,025 N (25 mN), sur un agitateur oscillant pendant 30 minutes. Le mélange obtenu est ensuite filtré avec un seringue-filtre de 0,45 µm et recueilli dans un flacon à scintillation de 7 mL, et conservé ainsi. Une partie de cet échantillon est ensuite prélevée, puis analysée par chromatographie d'échange de cations.
Nota : En fonction de la quantité d'échantillon disponible, la quantité utilisée pour l'analyse peut être modifiée, à condition que l'échantillon semble homogène et que le rapport poids d'échantillon/volume d'extraction reste le même (p. ex., 0,1g pour 10 mL de solution; soit 1:100). - On injecte 35µL d'échantillon dans une colonne analytique échangeuse de cations, qui permet la séparation de l'ion ammonium et des cations monovalents grâce à des groupements fonctionnels acide carboxylique/acide phosphonique. Afin de correctement résoudre l'ammonium du sodium et de réaliser son dosage, une solution d'acide sulfonique 0,003 N (3 mN) est utilisée comme phase mobile. Après l'élution de l'ion ammonium, les cations divalents et les amines quaternaires, qui pourraient interférer avec les analyses suivantes, sont éliminées en utilisant du H2SO4 avec un gradient de concentration allant de 0,2 N (200 mN) à 0,05 N (50 mN).
- La détection des cations est réalisée avec un détecteur de conductivité compensée fonctionnant en mode eau externe (CSRS-II). Cette méthode de détection permet de réduire la conductivité de fond due à la phase mobile et ainsi d'augmenter la sensibilité du détecteur pour l'analyte.
- Le dosage est réalisé par comparaison avec un étalonnage externe en cinq points, établi en mesurant la hauteur du pic dû au sulfate d'ammonium. La teneur en ammoniac (en µg/g de tabac entier) est calculée en multipliant la concentration d'ammoniac présente dans la solution analysée par le multiplicateur (10 mL) et le diviseur (g de tabac entier) appropriés. Les résultats de ce calcul sont exprimés en fonction de la « matière sèche ».
Nota : L'analyse et l'évaluation de certains produits à l'aide de cette méthode peuvent nécessiter l'utilisation de substances ou d'équipement potentiellement dangereux. Le présent document n'entend pas répondre à tous les aspects concernant la sécurité de son utilisation. Avant d'utiliser cette méthode normalisée, toute personne a la responsabilité de consulter les autorités compétentes et de prendre des mesures de protection de la santé et des mesures de sécurité qui tiennent compte des règlements en vigueur.
4 Appareillage et équipement
- Lyophilisateur.
- Agitateur oscillant.
- Balance analytique mesurant à la quatrième décimale au moins.
- Broyeur de laboratoire avec tamis no 40 (40 mailles au pouce carré).
- Filtre à seringue en fibre de verre de 25 mm × 0,45 µm.
- Fioles jaugées de 25, de 50 et de 100 mL.
- Seringue jetable de 5mL.
- Flacons de 7 mL à bouchon vissant recouvert d'aluminium.
- Septum, 8 mm, bleu, TFE/SIL, 60 MIL.
- Flacons de 2 mL pour échantillonneur automatique, avec bouchon.
- Chromatographe liquide à haute pression (CLHP) comprenant :
- Échantillonneur automatique réfrigéré à boucle de 100µL à remplissage partiel.
- Système permettant un gradient ternaire.
- Chauffe-colonne.
- Détecteur de conductivité Dionex ED-40 ou l'équivalent.
- Piège à cation Dionex CTC-1 ou l'équivalent.
- Compensateur de conductivité Dionex CSRS-II, en mode eau externe ou l'équivalent.
- Système de collecte de données.
- Colonne analytique échangeuse de cations Dionex IonPac CS12A (250 mm × 4 mm) ou l'équivalent.
- Colonne de garde échangeuse de cations Dionex IonPac CG12A ou l'équivalent.
- Erlenmeyers de 125 mL en polyméthylpentène (PMP) à bouchon vissant, et/ou tubes à culture de 16 mL à bouchon vissant en HDPE (en fonction du poids d'extraction et des volumes utilisés).
5 Réactifs et matériel
Nota : Tous les réactifs doivent être au moins de qualité réactif.
- Sulfate d'ammonium à pureté > 99 %.
- Acide sulfurique > 96 %.
- Acide méthanesulfonique (MSA) à 100 %.
- Eau de type I (conformément aux spécifications de la norme D 1193 de l'ASTM).
6 Préparation de la verrerie
- La verrerie doit être lavée et séchée de façon à s'assurer qu'elle ne causera aucune contamination.
- Immédiatement avant l'usage, tous les tubes à extraction sont lavés au H2SO4 0,1 N et rincés trois fois à l'eau désionisée et trois fois à l'eau de type I.
7 Préparation des solutions
- Solution d'acide sulfurique, 0,10 N - pour les solutions mères étalons
- Ajouter avec précaution 5,108 g de H2SO4 (96 % m/m) dans 900 mL d'eau de type I.
- Mélanger et diluer à 1 L avec de l'eau de type I.
- Solution d'acide sulfurique 0,025 N - pour l'extraction
- Ajouter avec précaution 1,277 g de H2SO4 (96 % m/m) dans 900 mL d'eau de type I.
- Mélanger et diluer à 1 L avec de l'eau de type I.
- Solution C : acide sulfurique 0,20 N - pour la chromatographie d'échange d'ions
- Ajouter avec précaution 10,216 g de H2SO4 (96 % m/m) dans 900 mL d'eau de type I.
- Mélanger et diluer à 1 L avec de l'eau de type I.
- Solution A : MSA 3 mN - pour la chromatographie d'échange d'ions
- Ajouter avec précaution 0,2883 g d'acide méthanesulfonique (MSA) dans 900 mL d'eau de type I.
- Mélanger et diluer à 1 L avec de l'eau de type I.
8 Préparation des étalons
- Préparation de l'étalon primaire (1e) d'ammonium :
- Peser exactement 0,20 g de sulfate d'ammonium dans une fiole jaugée de 50 mL.
- Dissoudre dans du H2SO4 0,10 N.
- Remplir la fiole au trait
- Préparer un étalon frais aux dix jours ouvrables.
Nota : Cette solution correspond à une solution mère renfermant 1,0898 mg/mL d'ion NH4+.
Le tableau suivant présente les étalons de travail pour 7 échantillons, y compris le volume de l’étalon d’ammonium, le volume final et la concentration des solutions mères étalons.
-
Étalons dilués Étalon
noVolume de sol. primaire
(µL)Volume Finale
(mL)Concentration
[µg/mL]0 0 25 0,000 1 250 25 10,898 2 175 25 7,6283 3 75 25 3,2693 4 75 50 1,6346 5 50 100 0,5449 6 20 100 0,2180
Nota : Tous les étalons dilués sont complétés avec du H2SO4 25mN. Préparer un étalon frais aux cinq jours ouvrables
Nota : Tous les poids, volumes et puretés doivent être notés et utilisés pour calculer exactement la concentration des étalons.
9 Échantillonnage
- L'échantillonnage des produits du tabac doit se faire conformément aux spécifications de la publication T-115.
10 Analyse des échantillons
- Préparation des échantillons
- Sécher le tabac entier dans un lyophilisateur pendant 48 heures.
- Broyer le tabac entier avec un broyeur muni d'un tamis de maille 40.
- Peser exactement 100 mg de tabac broyé dans un tube à culture de 16 mL.
- Ajouter 10 mL de solution d'extraction et agiter pendant 60 minutes sur un agitateur oscillant.
- Laisser décanter le mélange (environ une heure); filtrer la solution sur un filtre à seringue et recueillir le filtrat dans un flacon de 8 mL pour stockage, en ayant soin de rincer d'abord le flacon avec environ 1 mL d'échantillon.
- Mettre 250µL du filtrat directement dans un flacon de 2 mL pour échantillonneur automatique et y ajouter 1 000µL de solution d'extraction (diluée cinq fois).
Nota : Cette dilution représente la dilution standard requise pour la plupart des produits du tabac séchés à l'air chaud. Le filtrat obtenu avec d'autres produits du tabac peut nécessiter d'autres dilutions (ou aucune) pour rester dans la même gamme de concentration. Toutes les dilutions sont réalisées avec la solution d'extraction.
Nota : Les dilutions ne doivent pas nécessairement être réalisées de cette manière. Les dilutions réalisées avec des fioles jaugées peuvent s'avérer plus précises (mais aussi plus laborieuses et plus susceptibles de contamination).
- Analyse par chromatographie d'échange d'ions
- Conditions pour le Dionex ED-40
Compensateur de conductivité (SRS) : 100 mA
Échelle : 20 µS
Sortie : Déport
Décalage : 1 % de la pleine échelle. - Échantillonneur automatique : Volume injecté
- Analyser en utilisant une boucle d'échantillonnage à remplissage partiel de 100µL et un volume d'injection de 35µL et 60µL d'eaux de lavage pour purger complètement la boucle d'échantillonnage.
- Température de la colonne : 30 ºC.
- Phase mobile / Conditions pour le gradient (système de gradient ternaire)
Solvant A : MSA 3 mN
Solvant B : Eau de type I
Solvant C : H2SO4 0,2 N
Débit : 1,5 mL/minute
Gradient : Des ajustements mineurs peuvent s'avérer nécessaires en fonction de la condition de la colonne et de la résolution de l'analyte.
Le tableau suivant présente l’analyse chromatographique par échange d’ions, ainsi que la composition de la phase mobile et les conditions de gradient tertiaire, durant un essai de 25 minutes. Le temps d’équilibrage est de 9 minutes. Le débit est de 1,5 mL/min.
Temps
(minutes)Composition % A % B % C 0,00 100 0 0 13,00 100 0 0 13,01 0 80 20 14,00 0 80 20 14,01 0 90 10 19,00 0 90 10 19,01 0 99 1 20,00 0 99 1 25,00 99 1 0 25,00 Fin de l'analyse : Équilibrate Temps d'équilibrage : 9,00 minutes
- Conditions pour le Dionex ED-40
- Calculs
- Détermination du facteur de réponse
- Un étalonnage initial est réalisé par l'analyse des étalons préparés, en allant des fortes concentrations vers les faibles (en injectant le tout premier étalon au moins deux fois, jusqu'à l'obtention d'une réponse et d'un temps de rétention constants).
- Une courbe d'étalonnage est préparée en traçant la concentration de l'étalon en ion NH4 en fonction de la hauteur des pics donnés par le détecteur de conductivité.
- Le FR est égal à la pente de la droite calculée par régression linéaire (hauteur du pic/concentration).
- Calcul de la teneur en ion ammonium
NH4+ [µg/g] = [Hauteur de pic × vol. solv. d’extr. (mL) × vol. final (mL)] / [FR × masse utilisée (g) × vol. portion utilisée (mL)]
où le volume portion utilisé (mL) représente le volume transvasé dans le flacon à échantillonneur automatique.
Nota : Les résultats sont exprimés en fonction de la « matière sèche », puisque la masse utilisée est celle d'un échantillon sec. - Calcul de la teneur en ammoniac
NH3 [µg/g] = NH4+ [µg/g] × 17/18
dans laquelle 17/18 représente une correction pour le rapport entre les masses moléculaires de NH4+ et de NH3.
- Détermination du facteur de réponse
11 Contrôle de la qualité
- Chromatogramme typique
- Voir l'annexe 1.
- Paramètres de contrôle typiques
- Avant de traiter un échantillon, il faut s'assurer, par l'analyse d'un blanc de réactif (eau), qu'il n'existe aucune perturbation due à la verrerie, au système d'analyse et aux réactifs.
- Les échantillons à blanc doivent subir toutes les étapes de préparation et d'analyse.
- Pour chaque lot analysé, il faut analyser un blanc de réactif et une matrice fortifiée (MF). Les échantillons à blanc et les échantillons dopés (fortifiés) doivent subir toutes les étapes de préparation et d'analyse.
- Chaque lot d'échantillons doit comprendre un échantillon de tabac témoin dont la teneur en ammoniac est connue.
- Taux de récupération et niveaux de contamination
- Les taux de récupération typiques observés pour des blancs fortifiés (BF) et des matrices fortifiées (MF) se situent dans la gamme 85 - 110 %, lorsque les solutions dopées (ou les échantillons) sont soumises à tout le processus d'extraction.
- La valeur typique des blancs de réactifs est 0 µg/g. Une valeur > 0 µg/g signifie généralement une contamination du tampon filtre lors de son conditionnement ou à un mauvais rinçage de la verrerie.
- Limite de détection de la méthode (LDM) / Limite de dosage (LD)
- La limite de détection de la méthode (LDM) est déterminée par analyse, comme inconnu, de l'étalon de plus faible concentration au moins 10 fois pendant une période de plusieurs jours. La LDM est égale à trois fois l'écart-type de ces résultats.
- La LDM (exprimée en ng/g) peut être modifiée en faisant varier la quantité de tabac utilisée ou les volumes de solvant utilisés pour l'extraction et le nettoyage.
- La limite de dosage (LD) pratique est déterminée par analyse, comme inconnu, de l'étalon de plus faible concentration au moins 10 fois pendant une période de plusieurs jours. La LD est égale à 10 fois l'écart-type de ces résultats.
- Dans le cas d'échantillons réels, la traînée d'un énorme pic de sodium pouvant masquer la présence d'ions ammonium, la LDM et la LD dépendent de la résolution de l'analyse et de la quantité d'ions sodium présents dans l'échantillon.
- Stabilité des réactifs et des échantillons
- Des étalons primaires frais doivent être préparés aux 10 jours ouvrables et stockés à 4 ºC.
- Des étalons dilués frais doivent être préparés chaque semaine à partir des étalons mères et stockés à 4 ºC.
- Les échantillons sont stables pendant 48 heures à 4 ºC.
12 Références
- Risner, C.H. et Conner, J.M. Collection of Ammonia in Indoor Air by Means of a Weak Cation Exchange Cartridge. Environmental Toxicology and Chemistry, vol. 10, p. 1417-1423, 1991.
- Nanni, E.J., Lovette, M.E., Hicks, R.D., Fowler, K.W. et Borgerding, M.F. « Separation and Quantitation of Monovalent and Cationic Species in mainstream Cigarette Smoke Aerosols by High- Performance Ion Chromatography ». Journal of Chromatographic Science, vol. 28, août 1990.
- Colonne d'analyse IonPac CS12A, « Installation Instructions and Troubleshooting Guide », document no 031132, révision 01, Dionex Corporation, 1995.
13 Annexe
Annexe 1 : Chromatogramme typique
Cette figure présente un chromatogramme typique, où sont superposées les courbes obtenues avec un étalon et le tabac d’une cigarette témoin, avec un décalage de 5 %.
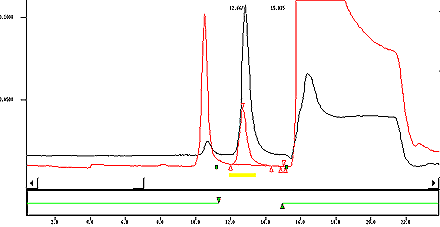
Superposition, avec décalage de 5 %, des chromatogrammes obtenus avec un étalon et le tabac d'une cigarette de référence.